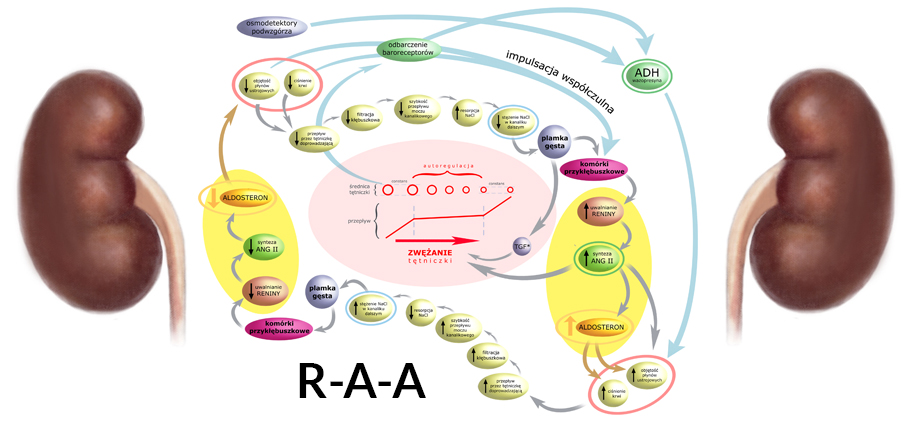
Regulacja Ciśnienia Krwi
Układ Renina-Angiotensyna-Aldosteron
Regulacja objętości płynów ustrojowych przez nerkę nie ogranicza się do wpływu wazopresyny na mechanizm zagęszczania lub rozcieńczania moczu. Drugim oddziaływaniem w którym nerka bierze czynny udział jest układ RAA (Renina-Angiotensyna-Aldosteron).
Przyjrzyjmy się przepływowi krwi przez nerkę.
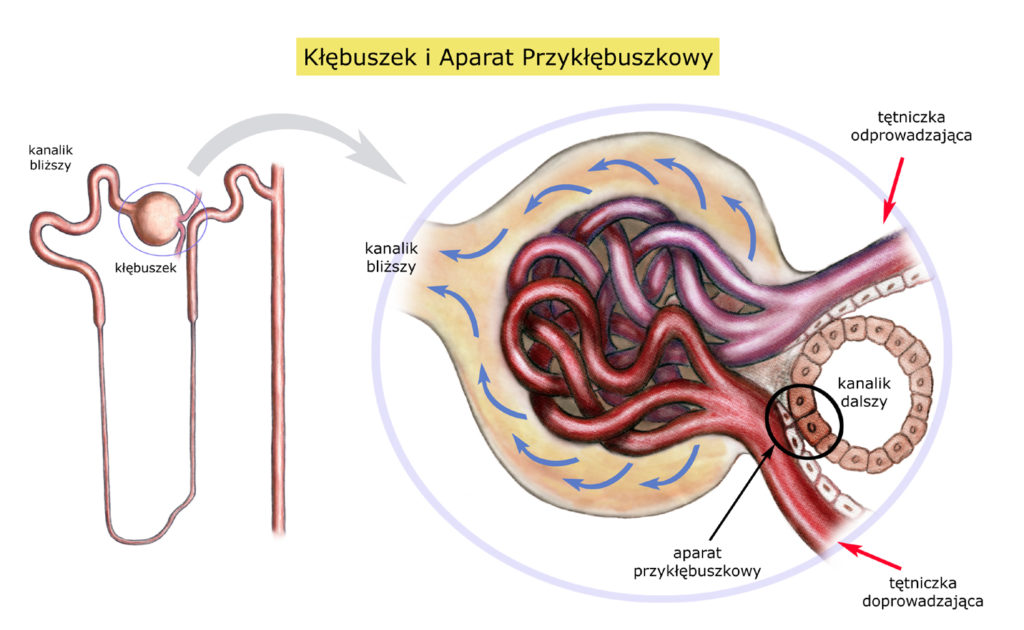
Tętniczka doprowadzająca krew do kłębuszka to niby zwykła tętniczka… a jednak niezwykła – istny fenomen wśród tętniczek. Spełnia rolę zaworu regulującego dopływ krwi do kłębuszków, a to oznacza, że – pośrednio – reguluje też ukrwienie całej nerki. Ale to nie wszystko! Komórki ściany tętniczki doprowadzającej produkują, gromadzą i uwalniają RENINĘ – ważny enzym układu RAA. Ale po kolei. Zacznijmy od autoregulacji.
Autoregulacja
Przepływu Krwi przez Nerkę
Wyobraź sobie, że „skoczyło” ci ciśnienie krwi. Z dowolnych powodów (choćby meczu piłkarskiego, w którym kolejny atak naszej drużyny kończy się rozpaczliwym podaniem do Szczęsnego). Taki skok ciśnienia powinien spowodować wzrost przepływu krwi przez nerkę, a więc również wzmożenie filtracji kłębuszkowej, zwiększenie produkcji przesączu i – co za tym wszystkim idzie – niekontrolowaną utratę wody i elektrolitów. Jednak tak się nie dzieje (!) – właśnie dzięki mechanizmowi autoregulacji przepływu krwi przez nerkę, w czym bierze udział tętniczka doprowadzająca.
Ściany tętniczki doprowadzającej działają jak reagujący na rozciąganie baroreceptor. Przy niskim ciśnieniu krwi tętniczka jest maksymalnie rozszerzona. Jeśli ciśnienie krwi rośnie, to od momentu przekroczenia progu 90 mm Hg – ściany tętniczki doprowadzającej zaczynają się zwężać, a więc zmniejsza się światło tętniczki – zwiększając tym samym opór naczyniowy. Dzięki temu przepływ krwi przez kłębuszki się nie zmienia: im bardziej rośnie ciśnienie, tym bardziej zmniejsza się światło tętniczki. Górną granicą jest 180 mm Hg.
Tak więc w zakresie 90 – 180 mm Hg tętniczka doprowadzająca zapewnia stałość przepływu krwi: im wyższe ciśnienie – tym węższa tętniczka; im niższe ciśnienie – tym szersza. Przy ciśnieniu 180 mm Hg tętniczka jest już maksymalnie zwężona, więc nie jest w stanie przeciwdziałać dalszym wzrostom ciśnienia.
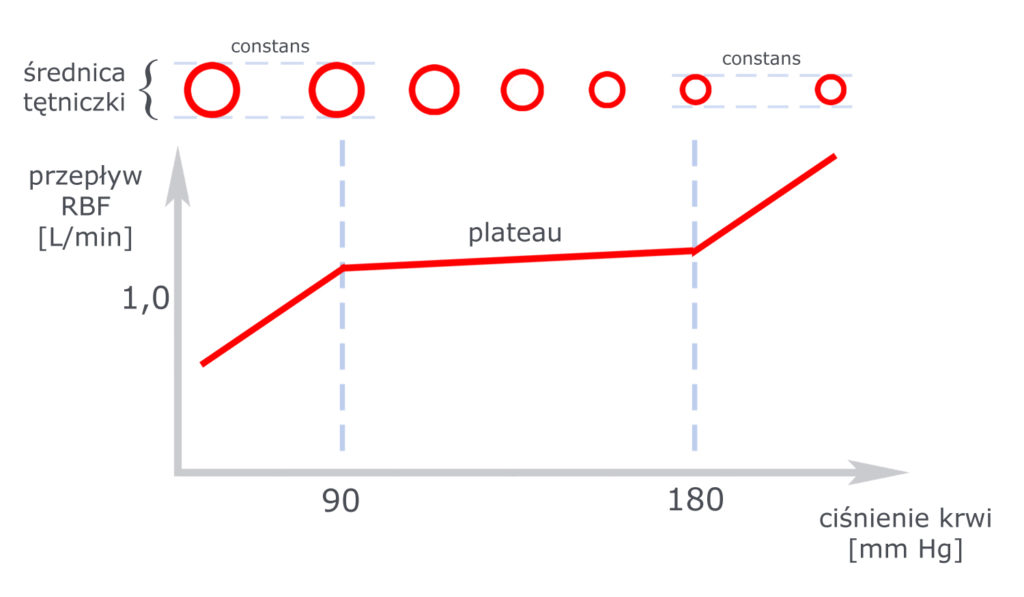
RBF (Reanal Blood Flow) to całkowity przepływ krwi przez nerkę. Jak widać autoregulacja uruchamia się, gdy przepływ osiąga nieco ponad litr krwi na minutę.
Mechanizm ten jest niezależny od unerwienia nerki (działa nawet po odcięciu od nerki wszystkich dochodzących do niej nerwów).
Opisana powyżej autoregulacja nie jest, rzecz jasna, jedynym mechanizmem regulującym nerkowe krążenie krwi i filtrację kłębuszkową. Duże znaczenie mają też wpływy SPOZA nerki, a więc wpływy nerwowe (impulsy układu współczulnego), hormonalne (m.in. układ renina-angiotensyna-aldosteron) i parakrynne. Zacznijmy od tych ostatnich.
Kanalikowo-Kłębuszkowe Sprzężenie Zwrotne
Mechanizmy parakrynne są to efekty powodowane przez tzw. autakoidy, czyli substancje powstające w samej nerce i działające lokalnie. Jedną z modyfikacji parakrynnych jest tzw. kanalikowo-kłębuszkowe sprzężenie zwrotne (TGF – Tubulo-Glomerular Feedback).
Aparat przykłębuszkowy tworzą:
A) ziarniste komórki tętniczki doprowadzającej (wydzielające reninę) oraz
B) komórki ‘plamki gęstej’ (macula densa) – wysokie, ciasno ułożone komórki kanalika dalszego.

Komórki plamki gęstej – reagują na zmiany stężenia NaCl wewnątrz kanalika dalszego. Jak pamiętasz z poprzedniego opracowania, w ramieniu wstępującym pętli nefronu odbywa się resorpcja NaCl:
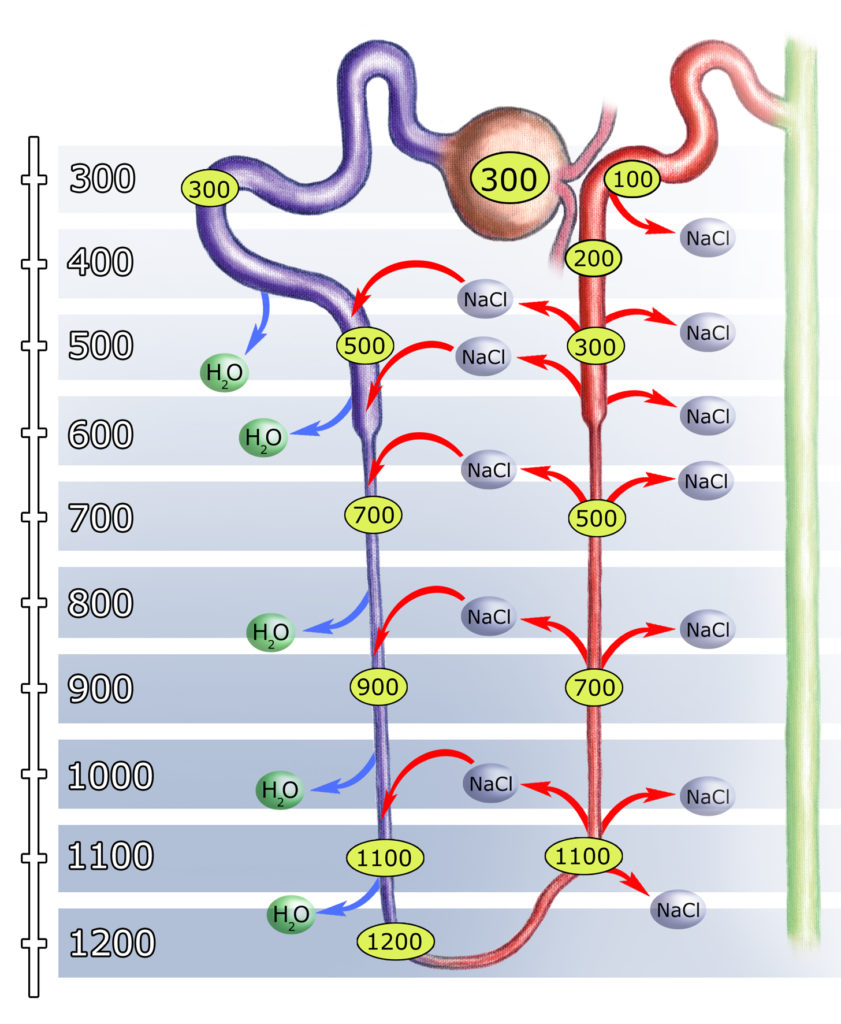
Jeśli przepływ moczu kanalikowego przez pętlę jest zbyt duży (zbyt szybki), to NaCl nie ulega resorpcji w pożądanej ilości; można powiedzieć, że ramię wstępujące pętli ‘nie nadąża’ z resorpcją.
Zwiększona ilość NaCl w świetle kanalika dalszego pobudza komórki plamki gęstej do syntezy czynnika parakrynnego (autakoidu), którym – prawdopodobnie – jest adenozyna. Adenozyna dociera lokalnie do komórek tętniczki doprowadzającej, powodując skurcz tętniczki doprowadzającej. Efektem tego jest zmniejszenie przepływu krwi przez kłębuszek i zmniejszenie filtracji kłębuszkowej, a więc również zmniejszenie szybkości przepływu moczu kanalikowego przez pętlę nefronu. Dzięki temu NaCl jest wydajniej resorbowany i jego stężenie w kanaliku dalszym spada.
Komórki plamki gęstej uczestniczą też w innym mechanizmie, a mianowicie wpływają na uwalnianie RENINY przez komórki przykłębuszkowe (a więc na układ RAA).
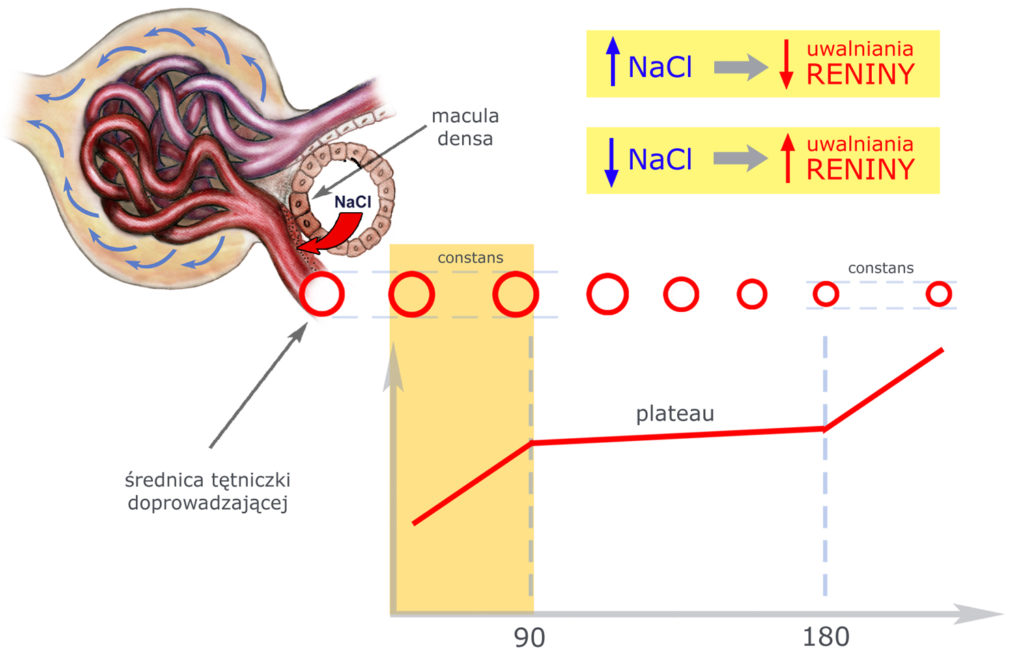
Na rysunku powyżej relację tę zaznaczono czerwoną strzałką.
1) Duże stężenie NaCl (w kanaliku dalszym) – HAMUJE uwalniania RENINY
2) Małe stężenie NaCl (w kanaliku dalszym) – ZWIĘKSZA uwalniania RENINY
Innym przykładem mechanizmu parakrynnego jest działanie prostaglandyn (PGI2 w kłębuszkach oraz PGE2 w rdzeniu nerki). Prostaglandyny te zapobiegają nadmiernemu zmniejszeniu przepływu krwi przez nerkę (gdyż neutralizują działanie wazopresyny i angiotensyny II).
Mechanizmy Nerwowe i Hormonalne
Wpływy nerwowe często współdziałają z hormonalnymi.
Unerwienie eferentne nerki (a więc doprowadzające impulsy do nerki) pochodzi ze zwojów pnia współczulnego. Zakończenia tych włókien nerwowych znajdują się m. in. właśnie w ścianach tętniczek doprowadzających (także w ścianach naczyń prostych).
Aktywacja układu współczulnego – np. w przebiegu intensywnego wysiłku fizycznego (a także w przypadku krwotoku lub wstrząsu) – współistnieje i współdziała z wyrzutem adrenaliny z rdzenia nadnerczy. Tak więc zarówno drogą impulsów współczulnych jak i drogą krwi poprzez adrenalinę – dochodzi do pobudzenia receptorów α-adrenergiczne w tętniczkach wewnątrznerkowych.
Efektem nr 1 jest więc ZWĘŻENIE tętniczek nerkowych, czyli obniżenie przepływu krwi przez nerkę (‘odcięcie’ nerki). Takie przekierowanie przepływu krwi z nerki na inne obszary bywa bardzo korzystne dla organizmu, gdyż dzięki temu w sytuacjach stresowych wzrasta ukrwienie mięśni, serca i mózgu.
Impulsy nerwów współczulnych powodują jednakże także Efekt nr 2, którym jest pobudzenie receptorów β-adrenergicznych aparatu przykłębuszkowego*. Prowadzi to do uwalniania RENINY przez ziarniste komórki tętniczki doprowadzającej, a więc aktywacji układu RAA.
*) Nerwy współczulne, których zakończenia znajdują się w komórkach przykłębuszkowych sprawiają, że nawet pozycja ciała miewa wpływ na uwalnianie reniny.
Podsumujmy co już wiemy. Mamy do czynienia z:
1. Autoregulacją w zakresie 90-180 mm Hg (skurcz tęt. dopr.)
2. Kanalikowo-kłębuszkowym sprzężeniem zwrotnym (skurcz tęt. dopr.)
3. Wpływ poziomu NaCl (w kanaliku dalszym) na uwalnianie reniny
4. Impulsacją współczulną
A) wpływy α-adrenergiczne (skurcz tętniczek wewnątrznerkowych)
B) wpływy β-adrenergiczne – uwalnianie reniny
Już na pierwszy rzut oka widać, że istotnymi elementami autoregulacji i regulacji odruchowej są skurcz i renina – której uwolnienie też ostatecznie doprowadzi do skurczu. To od razu wskazuje na przewagę mechanizmów oszczędzających minerały i przeciwdziałających utracie wody.
* *
Regulacja Objętości Płynów Ustrojowych
/Układ Renina – Angiotensyna – Aldosteron/
Powróćmy na chwilę do schematu autoregulacji. Ściany tętniczki doprowadzającej reagują na rozciąganie i zaczynają się zwężać po przekroczeniu progu 90 mm Hg.
Pytanie brzmi: co się dzieje poniżej tego progu, kiedy tętniczka doprowadzająca jest maksymalnie rozszerzona?
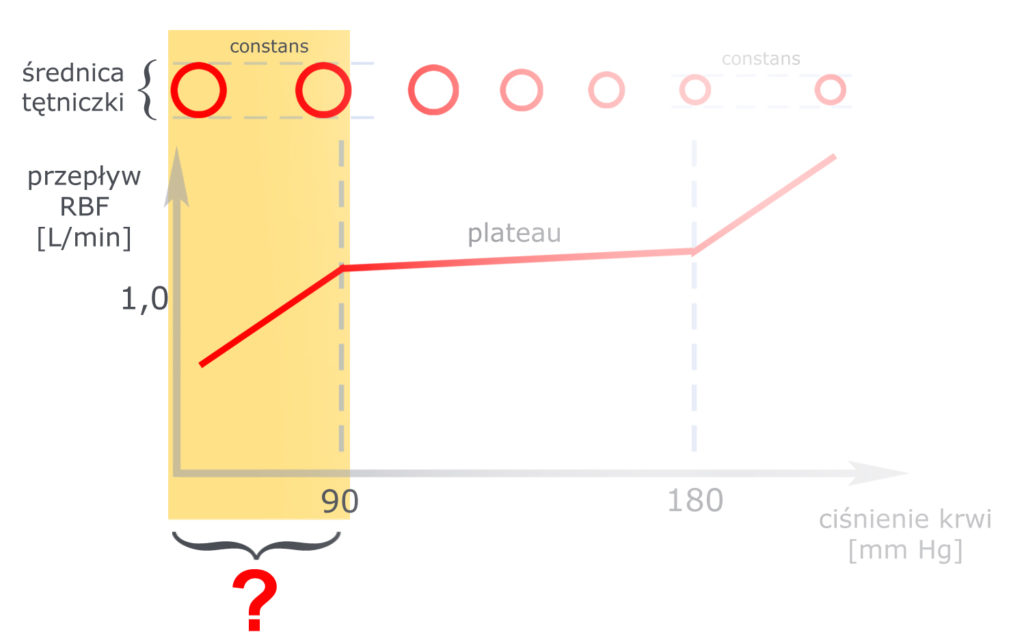
Nerka jest narządem czuwającym nad homeostazą, a więc również – a może wręcz przede wszystkim – nad objętością płynów ustrojowych. Maksymalne rozszerzenie tętniczki doprowadzającej jest sygnałem niskiego ciśnienia krwi, a więc alarmuje nerkę, że za chwilę nasz organizm może mieć tęgie kłopoty (łącznie z utratą przytomności).
Mówiliśmy o tym, że ściana tętniczki doprowadzającej jest baroreceptorem. Poniżej progu 90 mmHg ten baroreceptor jest całkowicie odbarczony, a odbarczenie baroreceptora zwykle wiążę się z ‘odhamowaniem’ układu współczulnego. A więc – na drodze odruchowej – wzrasta aktywność współczulna włókien unerwiających komórki przykłębuszkowe, pobudzając je do wydzielania RENINY.
Wyobraźmy sobie cały proces po kolei, dokładając kolejne elementy.
Stanem wyjściowym niech będzie moment, w którym ciśnienie krwi jest niskie, a ilość płynów ustrojowych niewystarczająca (odwodnienie). Słaby będzie też przepływ krwi przez tętniczkę doprowadzającą:
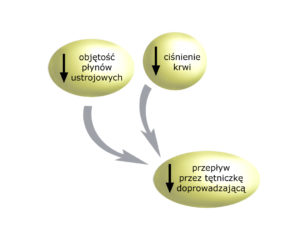
Zły przepływ przez tętniczkę oraz kłębuszek to mniejsza filtracja kłębuszkowa. Zmniejszenie szybkości przepływu moczu kanalikowego sprawi, że wzrośnie resorpcja NaCl w ramieniu wstępującym pętli nefronu. To spowoduje, że w świetle kanalika dalszego pojawi się niskie stężenie NaCl. Jest to ważny impuls dla komórek plamki gęstej (na rysunku zaznaczony błękitną elipsą).
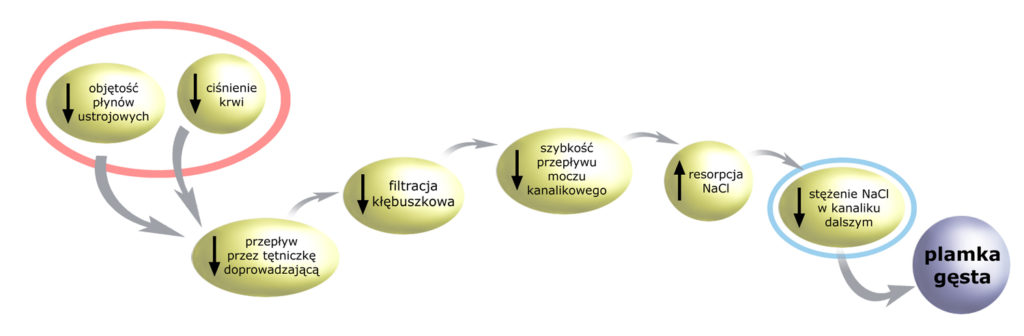
Ważny, ale nie jedyny, gdyż – przecież – pierwszą linią obrony naszego organizmu przed spadkiem ciśnienia krwi jest przeciwdziałanie odruchowe. Odbarczenie baroreceptorów tętniczych, m.in. w tętniczkach doprowadzających (oraz mechanoreceptorów sercowo-płucnych) powoduje odhamowanie układu współczulnego.
Impulsy współczulne powodują kurczenie się naczyń oporowych w narządach nie pracujących, a także skurcz mięśni gładkich dużych naczyń żylnych, głębokich żył skórnych i śledziony. Zwiększa się więc obwodowy opór naczyniowy, a rytm serca ulega przyspieszeniu (ze wzmocnieniem siły jego skurczu).
Nieco później dołącza – również odruchowa – autotransfuzja płynu tkankowego do łożyska naczyniowego. (Dzieje się tak, gdyż naczynia oporowe przedwłośniczkowe zwężają się bardziej niż pozawłośniczkowe; dzięki temu w naczyniach włosowatych przewagę zyskuje ciśnienie toniczne ‘wsysające’ płyn z tkanek do krwi.)
Impulsy współczulne działają też na komórki przykłębuszkowe. A więc uwalnianie reniny prowokowane jest i przez impulsację współczulną i przez spadek stężenia NaCl w kanaliku dalszym.
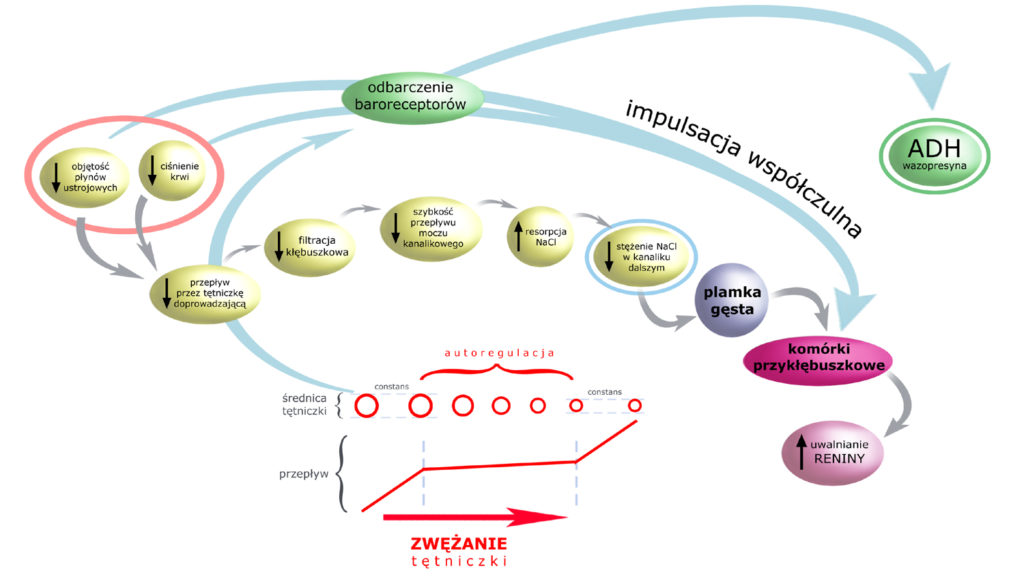
Odbarczenie baroreceptorów naczyniowych jest też impulsem do wyrzutu wazopresyny (ADH), która zaczyna zagęszczać mocz. Skoro jednak wspominamy o wazopresynie, na kolejnym obrazku zaznaczę też ‘rozkazy’ z osmodetektorów podwzgórza.
Renina jest enzymem proteolitycznym. Pojawiając się we krwi działa na angiotensynogen (jedno z białek krwi), ‘odcinając’ od niego fragment 10-aminokwasowy (dekapeptyd). Kiedy fragment ten (zwany angiotensyną I) dostaje się do krążenia płucnego, natrafia tu na inny enzym – konwertazę angiotensyny (ACE – angiotensin converting enzyme). ACE ‘odcina’ dwa kolejne aminokwasy, tworząc ostatecznie oktapeptyd – Angiotensynę II.
Angiotensyna II silnie kurczy naczynia TĘTNICZE, szybko – w ciągu kilku sekund – podnosząc ciśnienie krwi. Jednocześnie pobudza mechanizm pragnienia, działając na ośrodek pragnienia w podwzgórzu. Osobiście nasila wchłanianie sodu w kanalikach nerkowych, jednocześnie pobudzając korę nadnerczy do wydzielania ALDOSTERONU. I na koniec – skoro jest już we krwi – angiotensyna hamuje uwalnianie reniny z komórek przykłębuszkowych.
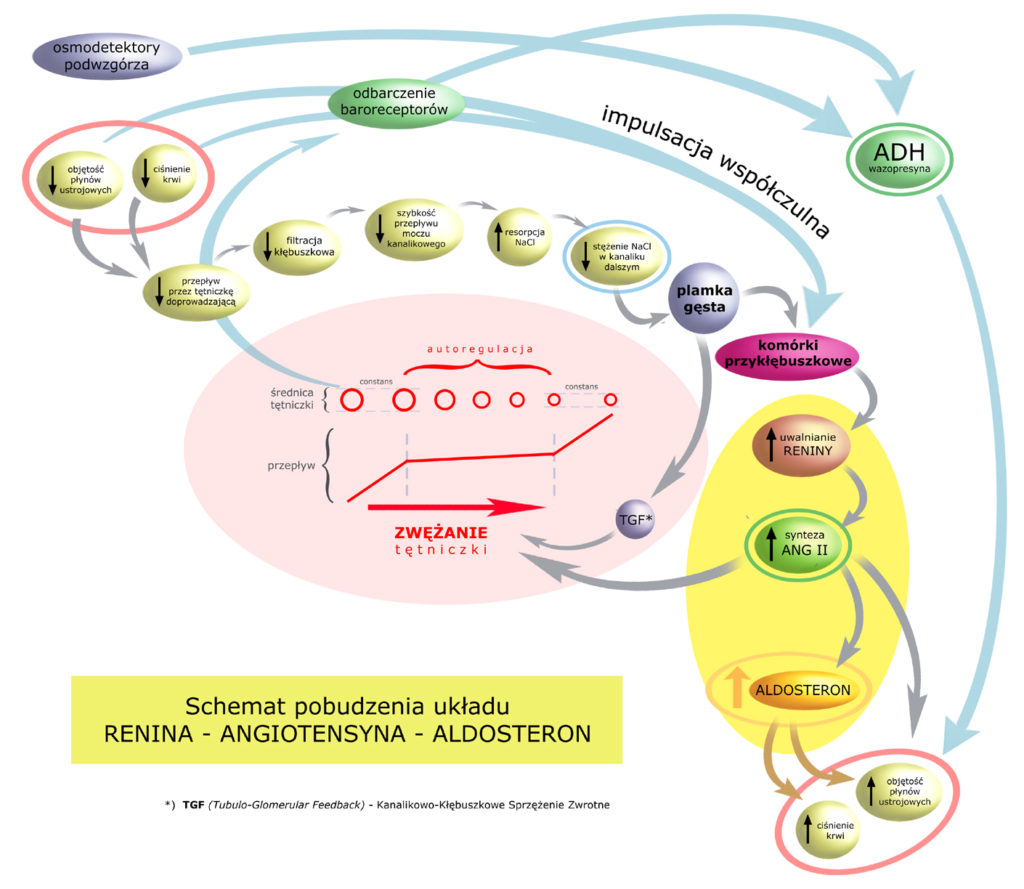
Na rysunku powyżej zaznaczyłem działanie kanalikowo-kłębuszkowego sprzężenia zwrotnego (TGF) oraz angiotensyny II – na tętniczkę doprowadzającą.
W tym miejscu mogą pojawić się niedomówienia…
Należałoby odpowiedzieć na pytanie: jak się mają do siebie oba mechanizmy wywoływane przez plamkę gęstą, tj. sprzężenie zwrotne TGF i pobudzanie układu renina-angiotensyna?
Wszystko wskazuje na to, że pomiędzy tymi mechanizmami nie ma żadnego związku czynnościowego, ponieważ:
A) W przypadku sprzężenia zwrotnego TGF mamy do czynienia raczej z regionalną autoregulacją resorpcji NaCl przez kanaliki w stosunku do szybkości filtracji kłębuszkowej, gdyż mechanizm ten aktywowany jest też w sytuacjach, gdy coś jest nie tak z resorpcją NaCl w kanaliku bliższym.
Natomiast:
B) Angiotensyna II działa ogólnie naczyniokurcząco (na cały nasz organizm), jednak nie na wszystkie tętniczki działa w równym stopniu. Na aparat przykłębuszkowy działa ona tak, że kurczy zarówno tętniczki doprowadzające jak i odprowadzające, jednak skurcz tętniczek odprowadzających jest mocniejszy, przez co filtracja kłębuszkowa nie ustaje – pomimo tego, że przepływ krwi przez nerkę staje się wyraźnie mniejszy.
Trzeba pamiętać, że zadaniem angiotensyny II jest w miarę szybkie podniesienie ciśnienia krwi, aby zapewnić perfuzję mózgu, serca i innych narządów. Jej działanie na nerkę w dużej mierze przypomina wpływy nerwowe układu współczulnego (‘odcięcie’ nerki). Na swoją obronę angiotensyna II ma to, że uruchamia i pragnienie i aldosteron, a więc czynniki, które za chwilę podniosą nam ciśnienie i przywrócą wszystko do normy.
Do pobudzenia układu renina-angiotensyna-aldosteron dochodzi przede wszystkim w przypadku zmniejszonej objętości płynów ustrojowych (odwodnienie) oraz obniżenia ciśnienia krwi. Przyczyną mogą też być wszelkie przypadki niedoboru NaCl (w tym także na diecie niskosodowej).
Na zakończenie tej części opracowania wypada jeszcze uzupełnić rysunek o sytuację, w której wazopresyna i aldosteron spełniły swoje zadanie… a nawet przedobrzyły:
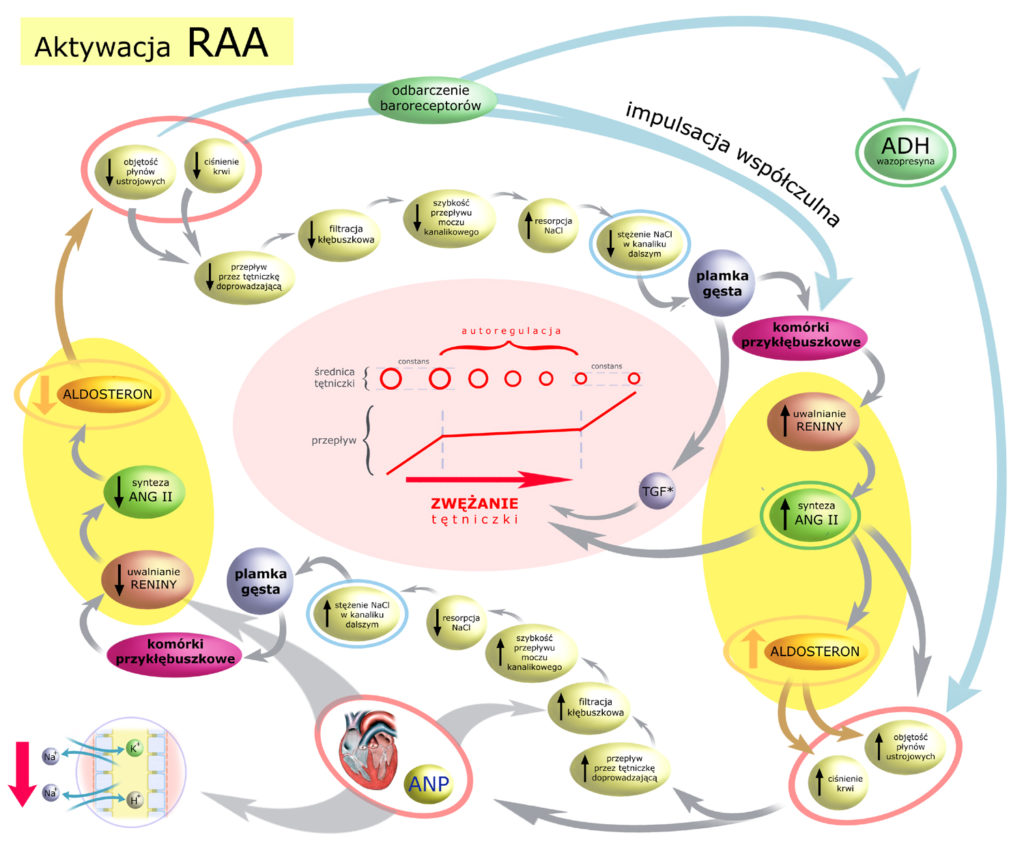
Powyżej uwzględniłem też działanie ANP (Atrial Natriuretic Peptide) – przedsionkowego peptydu natriuretycznego, o którym będzie mowa w opracowaniu opisującym działanie aldosteronu.
Na dzisiaj tyle.
Aldosteronowi przyjrzymy się… już niebawem 🙂