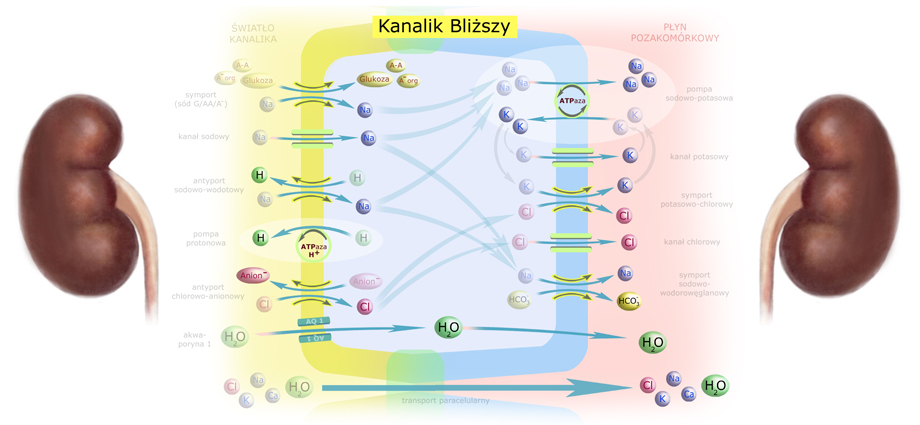
Kanalik Bliższy
(proksymalny)
Produktem filtracji kłębuszkowej jest przesącz (odbiałczone osocze), który – przepływając przez kanaliki nerkowe – zmienia swój skład, swoją osmolalność i swoje pH. Jest to efektem wymiany substancji pomiędzy światłem kanalików a otaczającym je śródmiąższem nerki, komunikującym się z krwią naczyń włosowatych. Tak więc osocze, które przedostaje się do torebki kłębuszka i dalej do kanalików, ostatecznie powraca do łożyska naczyniowego.
Z każdych 125 ml przesączu tylko 1 ml staje się moczem ostatecznym. Światło kanalików zasilają w największych ilościach – oprócz H2O – sód Na+, chlor Cl–, mocznik CO(NH2)2, wodorowęglany HCO3–, potas K+, wapń Ca2+ i fosforany HPO42-.
Głównymi składnikami moczu są NaCl i mocznik.
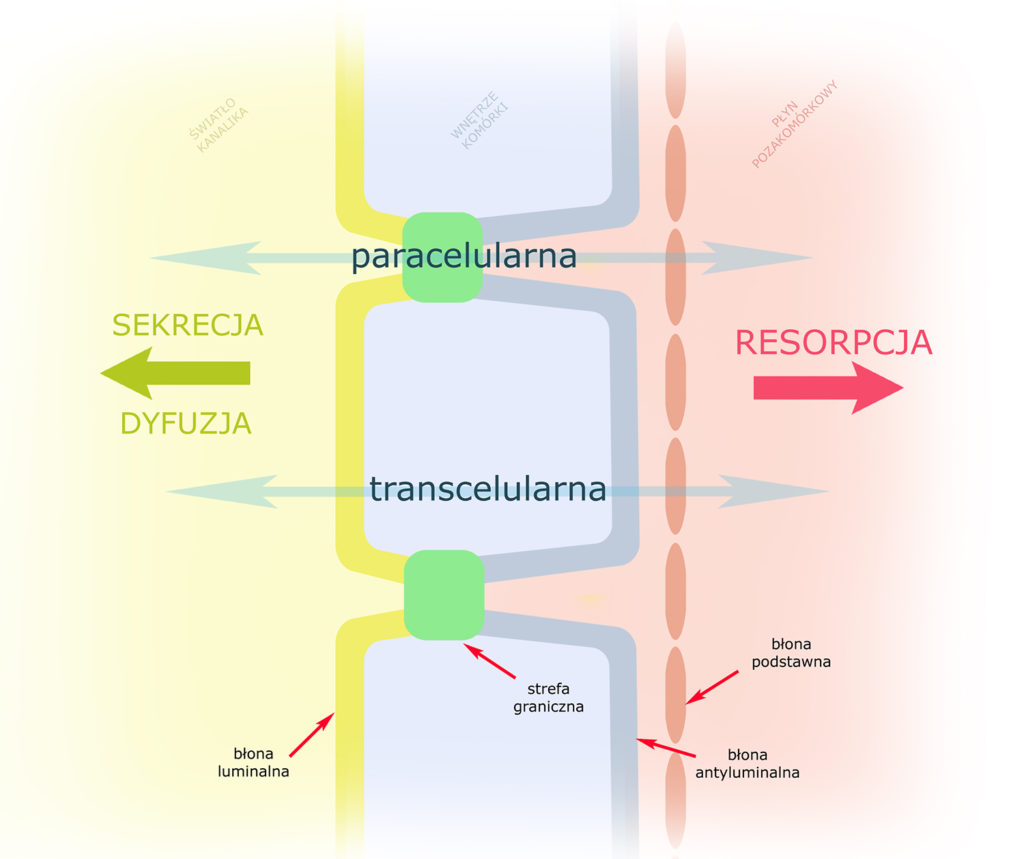
Istnieją dwie drogi przedostawania się substancji poprzez ściany kanalików: droga transcelularna (przezkomórkowa) i paracelularna (omijająca komórki). Droga transcelularna wymaga pokonania dwóch barier: błony luminalnej i antyluminalnej, natomiast paracelularna zachodzi poprzez złącza międzykomórkowe (strefy graniczne).
Zaznaczmy to na schemacie ściany kanalika nerkowego:
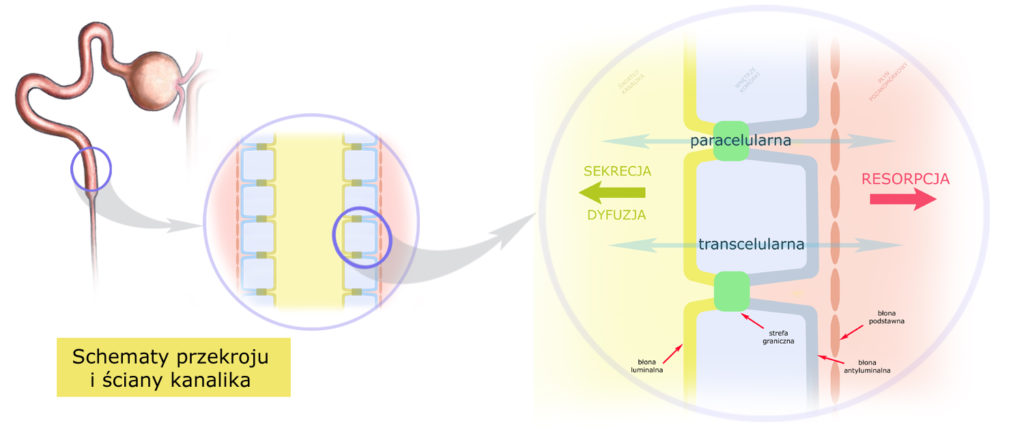
Transport kanalikowy (czyli ruch substancji przez ścianę kanalika) w kierunku od światła kanalika do śródmiąższu nazywamy resorpcją (albo reabsorpcją lub wchłanianiem zwrotnym). Ruch w kierunku przeciwnym, tj od śródmiąższu do światła kanalika, zwiemy sekrecją – gdy jest procesem czynnym, albo dyfuzją – gdy zachodzi w sposób bierny.
Zanim przypomnimy sobie ogólną wiedzę nt. transportu kanalikowego, zwróćmy uwagę na drogę paracelularną. Złącza międzykomórkowe miewają różną szczelność: w kanaliku bliższym są dobrze przepuszczalne (nabłonek przepuszczalny), a w ramieniu wstępującym pętli nefronu – bardzo szczelne. Przy dobrej przepuszczalności złącz międzykomórkowych woda płynie przez nie swobodnie, a nawet ‘porywa ze sobą’ substancje w niej rozpuszczone (co stanowi dodatkowy mechanizm transportu, o którym warto wiedzieć.)
Mechanizmy Transportu
DYFUZJA – zachodzi zgodnie z gradientami: gradientem chemicznym* (od większego do mniejszego stężenia substancji) lub – w przypadku jonów – gradientem elektrycznym (np. kationy dyfundują w kierunku środowiska elektroujemnego). Zauważ, że różnica gradientów jest pewnym potencjałem, a wiec rodzajem energii.
*) W przypadku wody zasada ta również jest zachowana (!), choć większość podręczników opisuje to w sposób nielogiczny i wprowadzający w błąd. Zwykle bowiem podkreśla się, że „woda dyfunduje w kierunku obszaru o większym stężeniu molarnym”. Zdanie to sugeruje, że dyfuzja zachodzi wbrew gradientowi stężeń. Jednak to nieprawda, gdyż odwołujemy się tu do stężenia molarnego substancji rozpuszczonej (!), a nie wody.
Po co – opisując coś, co dyfunduje – odwoływać się do stężeń czegoś, co nie dyfunduje? Zapewne po to, żeby utrudnić sobie życie.
Tymczasem:
Roztwór to mieszanina cząsteczek wody i cząsteczek substancji rozpuszczonej. Im więcej cząsteczek substancji rozpuszczonej, tym mniej cząsteczek wody. Tak więc ta sama treść co powyżej, zapisana we właściwy sposób, brzmi:
Woda dyfunduje zgodnie z własnym gradientem stężeń (a więc w kierunku obszaru o mniejszym stężeniu molarnym cząsteczek wody).
Jony zwykle dyfundują drogą transcelularną – kanałami jonowymi. Woda może dyfundować zarówno drogą paracelularną (przez złącza międzykomórkowe) jak i transcelularną – poprzez kanały wodne.
DYFUZJĘ (a więc transport zgodny z gradientami) nazywamy UŁATWIONĄ – gdy wykorzystuje ona przenośniki (transportery) białkowe. Zarówno kanałów jonowych, jak i wodnych zwykle nie zalicza się do transporterów, przyjmując, że są to ’białkowe szczeliny w błonach komórkowych’. Szczeliny te jednak miewają różnorakie konstrukcje i podlegają mechanizmom regulacyjnym nie mniej wyrafinowanym niż w przypadku regulacji działania przenośników.
* *
Transport CZYNNY to taki, który wykorzystuje energię inną niż energia gradientu stężeń. Zwykle pochodzi ona z hydrolizy ATP i nazywamy ją energią metaboliczną. Transport taki może być czynny pierwotnie i czynny wtórnie.
Transport czynny PIERWOTNIE zachodzi z bezpośrednim wykorzystaniem przenośników – enzymów zwanych ATP-azami. Tak więc energia wykorzystywana do transportu pochodzi wprost z hydrolizy ATP. Do przenośników takich należą:
ATP-aza Na+, K+ (tzw. ‘pompa sodowo – potasowa’)
ATP-aza H+, (tzw. ‘pompa protonowa’)
ATP-aza H+, K+ (tzw. ‘pompa protonowo – potasowa’)
ATP-aza Ca2+ (tzw. ‘pompa wapniowa’)
Transport czynny WTÓRNIE to taki, który byłby niemożliwy bez uprzedniego wykorzystania energii metabolicznej, jednak nie korzysta z niej bezpośrednio.
Załóżmy, że w efekcie działania pompy sodowo-potasowej (wykorzystującej hydrolizę ATP), po obu stronach błony komórkowej powstał bardzo duży gradient elektrochemiczny dla Na+. Jeśli teraz Na+ – zgodnie z gradientem stężeń – będzie powracał (kanałem jonowym) na drugą stronę błony komórkowej, to może on albo pociągnąć za sobą inny jon lub substancję (tzw. symport), albo też wymienić się z inną substancją, przerzucając ją na drugą stronę błony (tzw. antyport).
W błonach komórek kanalików – zarówno w błonach luminalnych jak i antyluminalnych – znajdują się mnogie układy przenoszące (wymieniacze jonowe, układy bramkujące kanały jonowe, układy umożliwiające podążanie wtórne jednych substancji za innymi). Te właśnie układy – wykorzystują energię metaboliczną WTÓRNIE, tj. bazują na wytwarzanych dzięki niej gradientach.
Kanalik Bliższy
/proksymalny/
W kanalikach bliższych resorpcji ulega 2/3 przesączu (~67%), przy czym nie zmienia on swojej osmolalności (resorbcja izoosmotyczna). Stężenia kationów Na+, K+ i Ca2+ nie ulegają zmianie, natomiast ilości anionów Cl– i HCO3– podlegają drobnej wymianie: nieco wzrasta stężenie Cl–, za to nieco maleje stężenie HCO3–.
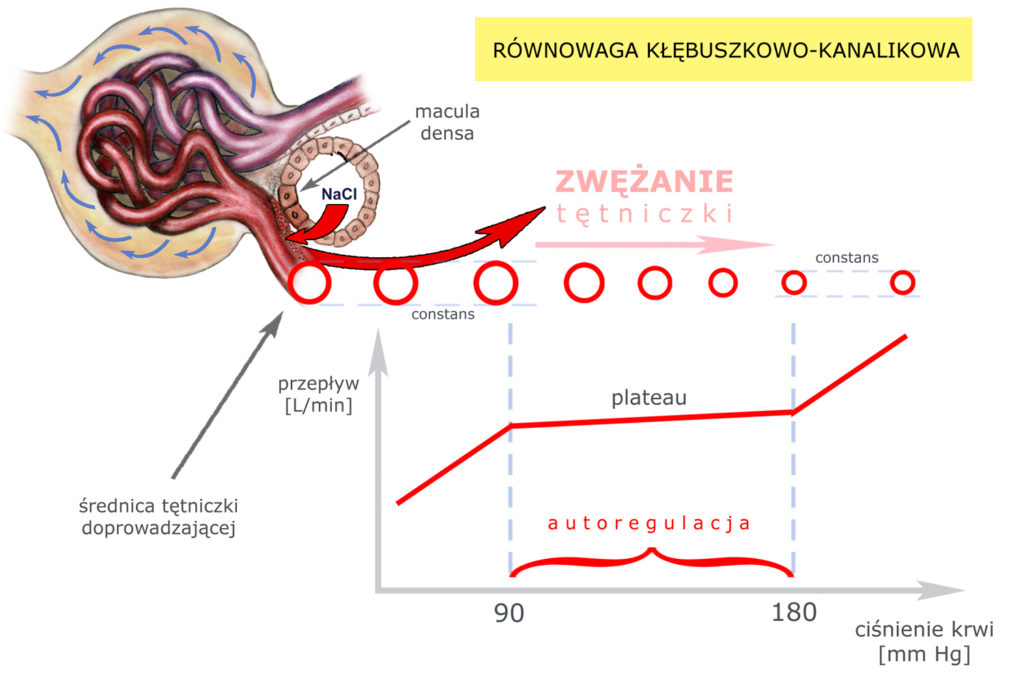
Równowaga Kłębuszkowo-Kanalikowa
Warto zatrzymać się nad mechanizmem regulującym wydajność resorpcji w kanalikach bliższych, gdyż – bez względu na zmiany ciśnienia krwi – zawsze jest ona proporcjonalna do wielkości filtracji kłębuszkowej GFR (Glomerular Filtration Rate). Zjawisko to nazywamy równowagą kłębuszkowo-kanalikową, a polega ono – po prostu – na tym, że jeśli spada filtracja kłębuszkowa, to spada też resorpcja w kanaliku bliższym; jeśli filtracja rośnie, to rośnie też resorpcja. W efekcie procentowy stosunek resorpcji do filtracji balansuje w dość wąskich granicach (67% do 70%).
Mechanizm ten jest bardzo istotny, gdyż zapobiega wahaniom tzw. ładunku dystalnego, a więc tej części przesączu, która nie jest resorbowana w kanaliku bliższym i przedostaje się do kanalika dalszego (dystalnego). Ładunek ten powinien stanowić 1/3 (~33%) przesączu, gdyż tylko to zapewnia sprawne funkcjonowanie dalszego odcinka nefronu.
Zbyt obfity ładunek dystalny spowodowałby ‘zalanie’ kanalika dalszego, który nie jest przystosowany do resorbowania tak dużych objętości płynu kanalikowego; doprowadziłoby to do utraty z moczem znacznych ilości wody i elektrolitów. Z kolei zbyt mały ładunek dystalny mógłby ulec wchłonięciu w całości, co odbierałoby nerce funkcjonalność jako narządu regulującego wydalanie i homeostazę.
Jakie mechanizmy mają swoją rolę w kształtowaniu równowagi kłębuszkowo-kanalikowej? Otóż równowaga ta jest zjawiskiem wewnątrznerkowym, niezależnym zarówno od impulsacji nerwowej jak i od regulacji hormonalnej. W kształtowaniu tej równowagi mogą więc brać udział A) wpływy parakrynne, a więc kłębuszkowo-kanalikowe sprzężenie zwrotne (TGF – Tubulo-Glomerular Feedback), oraz B) wpływy miogenne odpowiedzialne za autoregulację przepływu krwi przez tętniczkę doprowadzającą.
Jak pamiętasz z poprzednich opracowań TGF polega na tym, że rosnące stężenie NaCl w świetle kanalika dalszego (zbyt duży ładunek dystalny) pobudza komórki plamki gęstej do syntezy autakoidu (prawdopodobnie adenozyny), który – docierając lokalnie do komórek tętniczki doprowadzającej – powoduje jej skurcz. Efektem tego jest zmniejszenie przepływu krwi przez kłębuszek, zmniejszenie filtracji kłębuszkowej i zmniejszenie ładunku dystalnego.
Autoregulacja natomiast uniezależnia przepływ krwi przez kłębuszek od wahań ciśnienia krwi (w zakresie 90 – 180 mm Hg). W miarę wzrastania ciśnienia krwi mięśniówka tętniczki automatycznie zmniejsza jej światło, co zabezpiecza względną stałość przepływu krwi przez kłębuszek.
* *
Resorpcja
w Kanaliku Bliższym
Główną siłą napędową transportu zachodzącego w kanaliku bliższym jest – zlokalizowana w błonie antyluminalnej – tzw. POMPA SODOWO-POTASOWA (czyli enzym ATP-aza Na+/K+). Od tego więc zacznijmy:

Pompa sodowa utrzymuje wysokie stężenie sodu w przestrzeni pozakomórkowej, zaś niskie jego stężenie wewnątrz komórek ściany kanalika. To niskie stężenie sodu w cytoplazmie sprawia, że sód usiłuje się przedostać ze światła kanalika nerkowego – do wnętrza komórki.
Drugim ważnym zadaniem pompy sodowej jest utrzymywanie elektroujemności wnętrza komórek – zarówno w stosunku do światła kanalika jak i względem śródmiąższu nerki. Dzieje się tak, gdyż ‘wypompowuje’ z komórki więcej kationów (3 jony Na+) niż do niej ‘wpompowuje’ (2 jony K+). Każdy cykl działania pompy dba więc o to, aby wewnątrz komórki panował lekki niedobór kationów.
Umieśćmy pompę sodowo-potasową w rogu komórki, aby przedstawić losy innych jonów i substancji. Na początek: co dzieje się z wpompowanym do cytoplazmy potasem? Aby mógł być tam ponownie wpompowany (w kolejnym cyklu pracy pompy) – musi stamtąd najpierw uciec. Ucieka dwoma drogami: przez kanał potasowy i symporter (kotransporter) K+/Cl–:
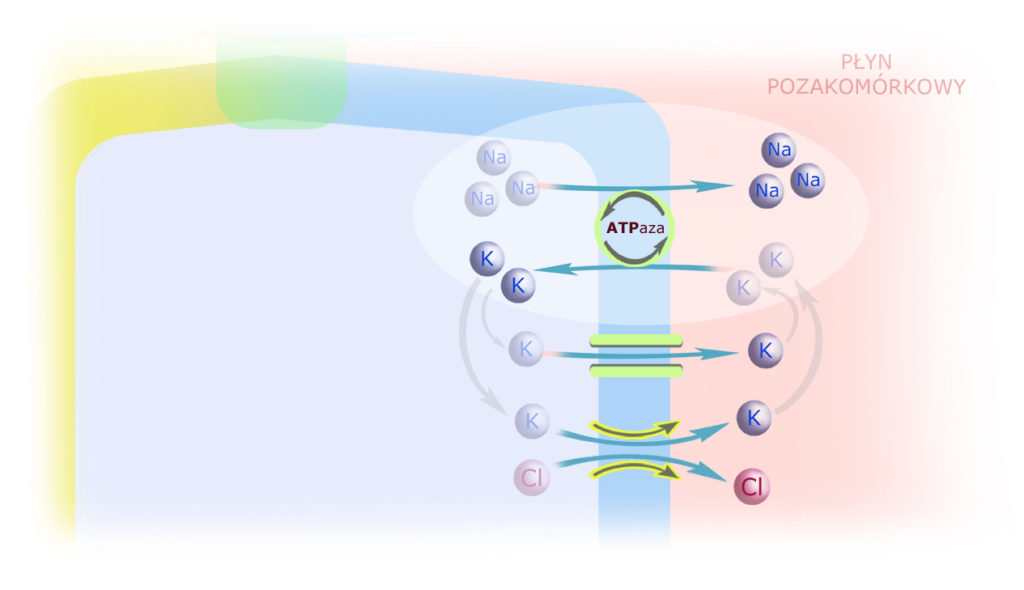
Teraz odpowiedzmy na pytanie: skąd biorą się te 3 jony sodu używane przez pompę sodowo-potasową? Wiemy już, że przyciągane są przez – wywołany pracą pompy – gradient stężeń, ale jaki mechanizm przerzuca je do cytoplazmy? Otóż w pierwszym odcinku kanalika bliższego mechanizmem tym jest symport sodu wraz z glukozą, aminokwasami (A-A), mleczanami i innymi anionami organicznymi (A– org)*:
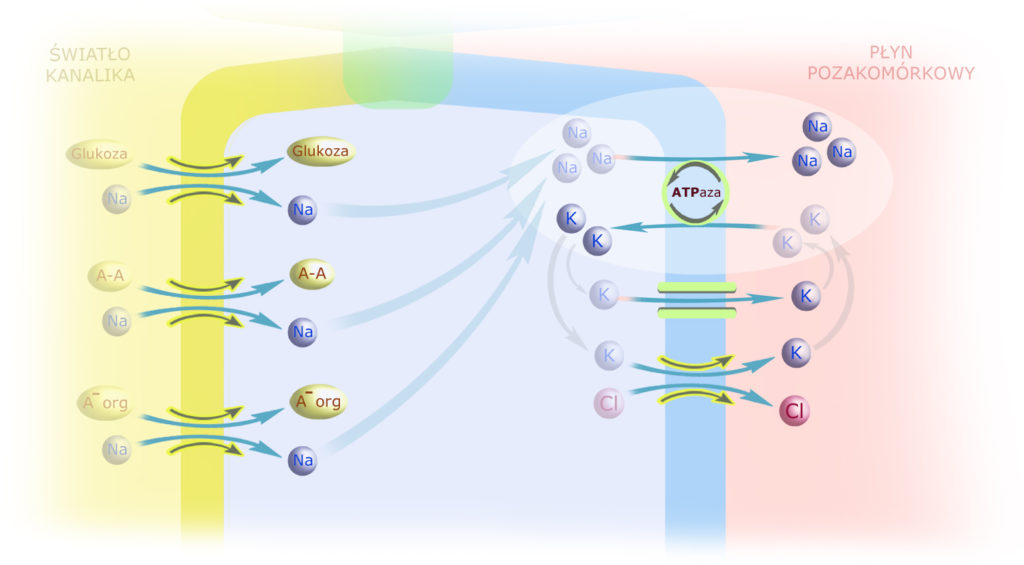
*) Nieco więcej o symporcie tych substancji w kanaliku bliższym – na końcu niniejszego artykułu.
W dalszej części kanalików bliższych sód przedostaje się do cytoplazmy również za pośrednictwem kanału sodowego oraz antyportu Na+/H+.
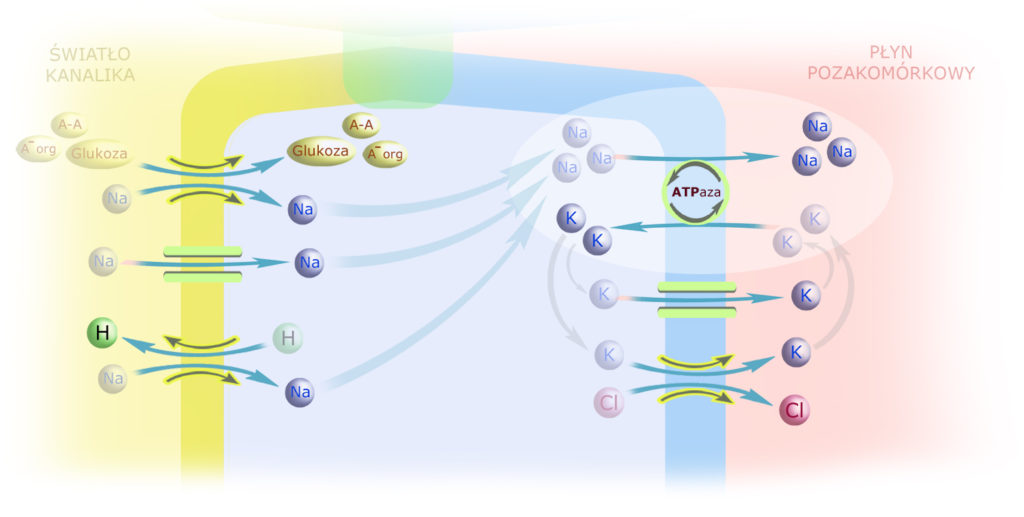
Działanie antyporterów Na+/H+ oraz Cl–/Anion–, a także wyrzut HCO3– do śródmiąższu (który dodatkowo napędza napływ sodu ze światła kanalika do cytoplazmy) i usuwanie H+ do światła kanalika (pompa protonowa) – mają związek z rolą nerek w regulacji równowagi kwasowo-zasadowej. (Przyjrzymy się temu już niebawem). Uzupełnijmy schemat o te elementy oraz kanał chlorowy w błonie antyluminalnej:

Na schemacie brakuje jeszcze co najmniej dwóch ważnych elementów: kanałów wodnych (akwaporyny typu 1) oraz transportu drogą paracelularną.
Powiedzieliśmy wcześniej, że złącza międzykomórkowe miewają różną szczelność, ale w kanaliku bliższym są akurat dość dobrze przepuszczalne. Przestrzenią międzykomórkową przemieszcza się więc woda oraz część jonów – zgodnie z istniejącymi gradientami: (elektrycznym, chemicznym, osmotycznym) oraz na zasadzie przepływu konwekcyjnego (solvent drag). O przepływie konwekcyjnym mówimy wtedy, gdy skomasowany przepływ (bulk flow) wody ‘porywa ze sobą’ substancje w niej rozpuszczone – czasem nawet wbrew gradientom.
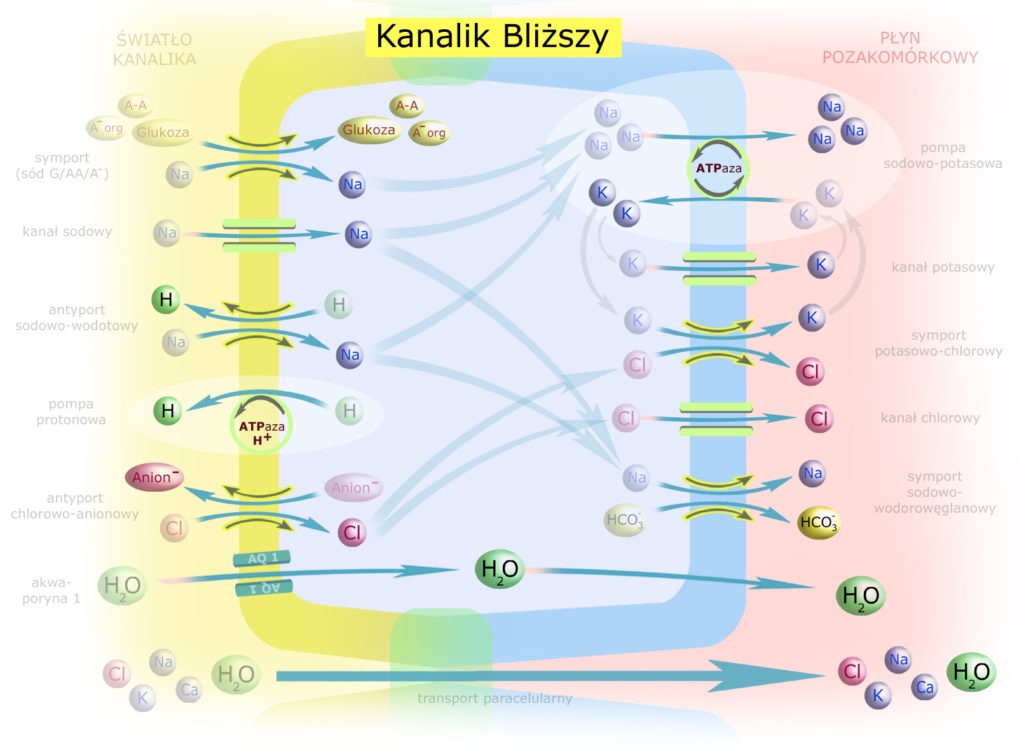
Omawiając transport na wysokości kanalików bliższych trzeba pamiętać, że zachodzi tu proces na wielką skalę: resorpcji ulega 2/3 objętości przesączu.
Zwróć uwagę na globalny kierunek przepływu. Potas krąży pomiędzy cytoplazmą i śródmiąższem, a do światła kanalika przenikają jedynie te jony, które uczestniczą w regulacji równowagi kwasowo-zasadowej (wodór + aniony, których chcemy się pozbyć). Wszystko inne ulega resorpcji na ogromną skalę. Dotyczy to 2/3 ładunku Na+, Cl– i wody oraz – niemal w całości – przesączonej glukozy, aminokwasów, związków organicznych, K+, Ca2+, wodorowęglanów i fosforanów*. Mocznik – ulega resorpcji w 50% (nie zostało to uwzględnione na schemacie).
*) Praca symportera sodowo-fosforanowego (również nie uwzględnionego na schemacie) regulowana jest hormonalnie: PTH (parathormon) ją hamuje a aktywna postać wit. D (kalcytriol) – pobudza.
Resorpcja na tak dużą skalę możliwa jest dzięki temu, że podczas filtracji kłębuszkowej białka osocza pozostały w łożysku naczyniowym. Białka te znajdują się teraz w naczyniach włosowatych okołokanalikowych, tworząc różnicę ciśnień tonicznych pomiędzy krwią a śródmiąższem nerki. Woda wsysana jest więc do naczyń z śródmiąższu, a śródmiąższ wsysa wodę z kanalików – drogą transcelularną (poprzez akwaporyny typu 1) oraz paracelularną (poprzez przepuszczalne strefy graniczne/złącza międzykomórkowe) wraz z rozpuszczonymi w niej jonami.
Dodatkowa energia dla resorpcji dostarczana jest przez pompę sodowo-potasową, która – budując różnicę gradientu sodowego – stwarza warunki dla transportu wtórnie czynnego, wykorzystującego ruch jonów sodu. Przemieszczanie się jonów do śródmiąższu pogłębia różnicę ciśnień tonicznych pomiędzy nim a światłem kanalika.
Siłami czuwającymi nad wydajnością resorpcji są (A) równowaga kłębuszkowo-kanalikowa i (B) ciśnienie krwi. Zwiększenie ciśnienia tętniczego nie tylko uruchomi (B1) autoregulację przepływu przez tętniczkę doprowadzającą, ale też (B2) utrudni ewakuację zresorbowanego płynu z śródmiąższu do naczyń włosowatych.
Dzieje się tak, gdyż ciśnienie hydrostatyczne w naczyniach krwionośnych – zawsze rywalizuje z ciśnieniem osmotycznym: hydrostatyczne – wypycha wodę, a osmotyczne – przyciąga ją. Mechanizmowi temu przypisuje się KLUCZOWĄ ROLĘ w długofalowej regulacji ciśnienia krwi.
Bo:
Uogólniony wzrost ciśnienia krwi pociąga za sobą, kolejno:
– wzrost ciśnienia w naczyniach wewnątrznerkowych,
– wzrost ciśnienia w śródmiąższu nerki,
– hamowanie resorpcji z kanalików,
– zwiększone wydalanie sodu i wody,
– zmniejszenie zawartości NaCl w ustroju,
– spadek objętości płynu pozakomórkowego,
– normalizacja ciśnienia krwi.
Ramię Zstępujące
Losy przesączu w kanaliku bliższym określa się jako ’izoosmotyczna redukcja objętości’ albo ‘resorpcja izoosmotyczna’. Trzeba pamiętać, że sformułowanie to dotyczy wyłącznie kanalików bliższych mniej więcej na wysokości kłębuszków. Ciśnienia osmotyczne zarówno przesączu jak i śródmiąższu nerki są tu identyczne (~300 mmol/kg), a mimo to dochodzi redukcji 2/3 objętości przesączu.
W zstępującej części nefronu – o jakiejkolwiek izoosmotyczności nie może już być mowy, gdyż na tym odcinku toniczność przesączu zwiększa się aż 4-krotnie (do ~1200 mmol/kg).
Spójrzmy na zestawienie schematu warstwowego rozkładu ciśnień osmotycznych nefronu, przepuszczalności ścian kanalików dla wody, oraz tego co dzieje się na każdym z poziomów.
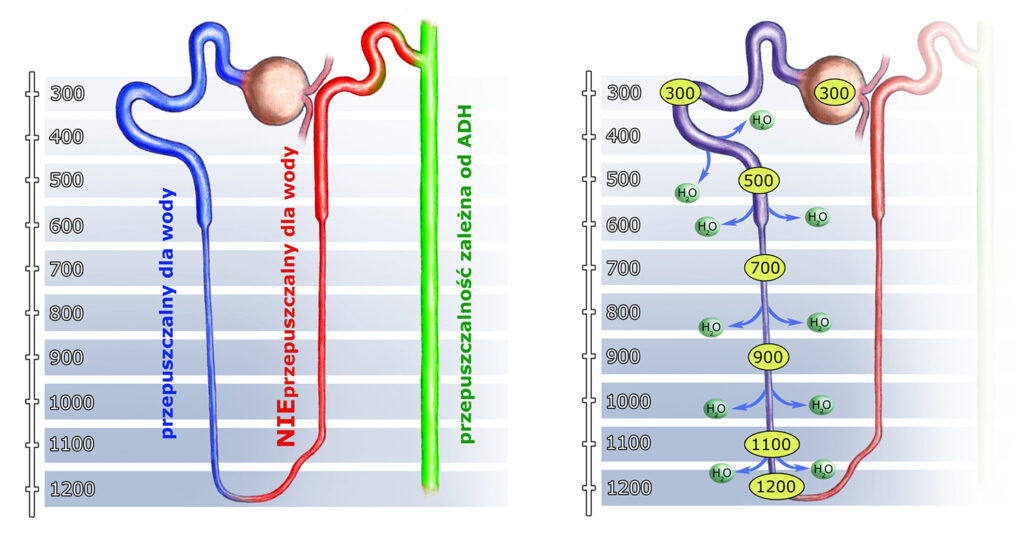
Niebieskim kolorem zaznaczyłem ten odcinek nefronu, którego ściany kanalików są przepuszczalne dla wody. Dzieje się tak z dwóch powodów: dlatego, że w błonach komórek znajdują się kanały wodne (tzw. akwaporyna typu 1) oraz dlatego, że na tym odcinku przepuszczalne dla wody są też złącza międzykomórkowe. Kolor czerwony markuje odcinek, gdzie oba te zjawiska nie występują, (tj. błony komórek nie zawierają akwaporyn, a złącza są wodoszczelne), natomiast kolorem zielonym oznaczono przepuszczalność warunkową – zależną od obecności hormonu antydiuretycznego. Na odcinku tym ADH ‘wbudowuje’ (lub ‘nie wbudowuje’ gdy go nie ma) w błonę komórkową kanały wodne zwane akwaporyną typu 2 (które – przy braku ADH – luźno pływają w cytoplazmie komórek).
Jak widać osmotyczność (gęstość) śródmiąższu nerki ułożona jest warstwowo. Jeśli więc mówimy jednocześnie o zagęszczaniu przesączu i o izoosmotyczności (na odcinku ramienia zstępującego), to jedynie w tym sensie, że przesącz – przemieszczając się przez ramię zstępujące – dąży do izoosmotyczności w stosunku do śródmiąszu nerki na każdym z poziomów odrębnie. Dążenie to sprawia, że – przesuwając się z poziomu na poziom – ‘stopniowo’* ulega on zagęszczaniu, pozbywając się wody.
*) Jeśli przesącz o gęstości 300 mmol/kg przesunie się w dół, to będzie sąsiadował z śródmiąższem o gęstości np. 500 mmol/kg. Śródmiąższ jest teraz hipertoniczny w stosunku do przesączu, więc woda będzie ‘wysysana’ ze światła kanalika (przez akwaporyny typu 1 i nieszczelne złącza międzykomórkowe ścian kanalików) do śródmiąższu.
Po chwili przesącz staje się prawie-izotoniczny w stosunku do tej warstwy śródmiąższu, która właśnie go otacza. Jednak od razu przesuwa się niżej i znów sąsiaduje z gęstszym śródmiąższem, więc wszystko zaczyna się od nowa: woda znów jest ‘wysysana’ – dążąc do osiągnięcia izotoniczności z kolejną warstwą śródmiąższu. I tak dalej.
Tak naprawdę więc przesącz nie jest izotoniczny ze śródmiąższem praktycznie w żadnym momencie; jedynie dąży do tej izotoniczności – co jest właśnie przyczyną pozbywania się wody.
Wydajność zagęszczania przesączu w ramieniu zstępującym nefronu rośnie dzięki mechanizmowi wzmacniania przeciwprądowego. W grę wchodzi więc nie tylko wysysanie wody do przestrzeni okołokanalikowej, ale też wnikanie (dyfuzja) jonów Na+ i Cl– do światła kanalików.
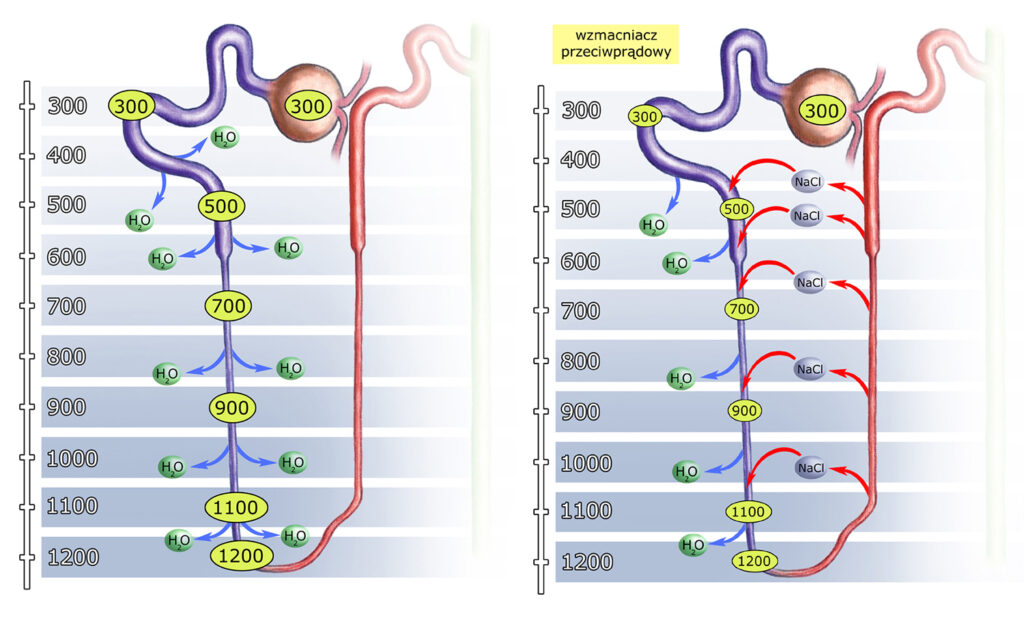
Wzmacnianie przeciwprądowe dotyczy także cząsteczek mocznika CO(NH2)2 (co nie zostało oznaczone na powyższym obrazku).
Ramię Wstępujące
Błony komórkowe ścian kanalików ramienia wstępującego nie zawierają akwaporyn, a ich złącza międzykomórkowe nie są przepuszczalne dla wody… ALE (!) złącza te są przepuszczalne dla sodu.
Na wysokości pętli nefronu przesącz jest zagęszczony do wartości ~1200 mmol/kg. Teraz – przemieszczając się ramieniem wstępującym – przesącz, a właściwie już mocz kanalikowy – ulega rozcieńczaniu. W początkowym – cienkim – odcinku ramienia wstępującego zachodzi jedynie resorpcja bierna: sód przedostaje się do śródmiąższu zgodnie z gradientem stężeń – właśnie poprzez złącza międzykomórkowe. Ruch ten napędzany jest przemieszczaniem się jonów chloru przez błonowe kanały chlorowe.
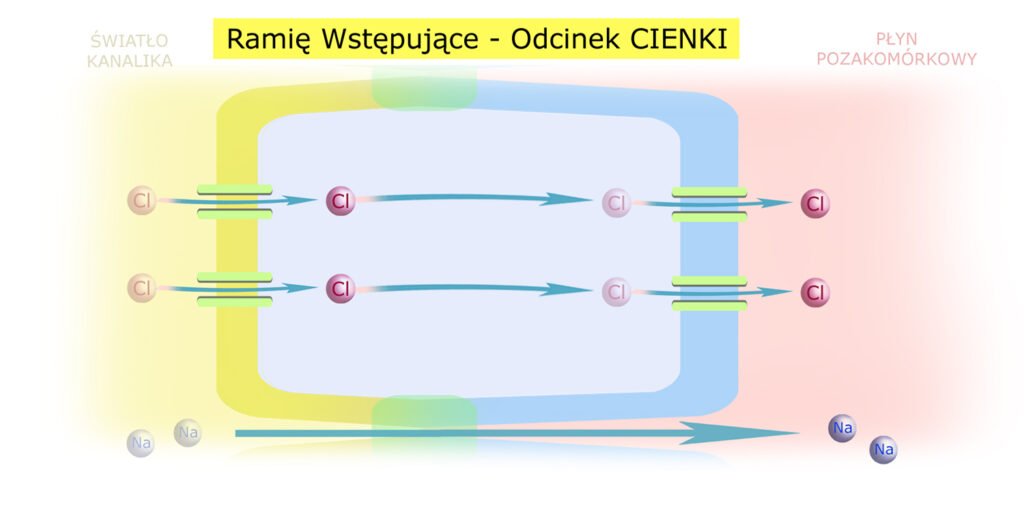
W grubym odcinku ramienia wstępującego dołącza transport czynny, zasilany – rzecz jasna – przez pompę sodowo-potasową:
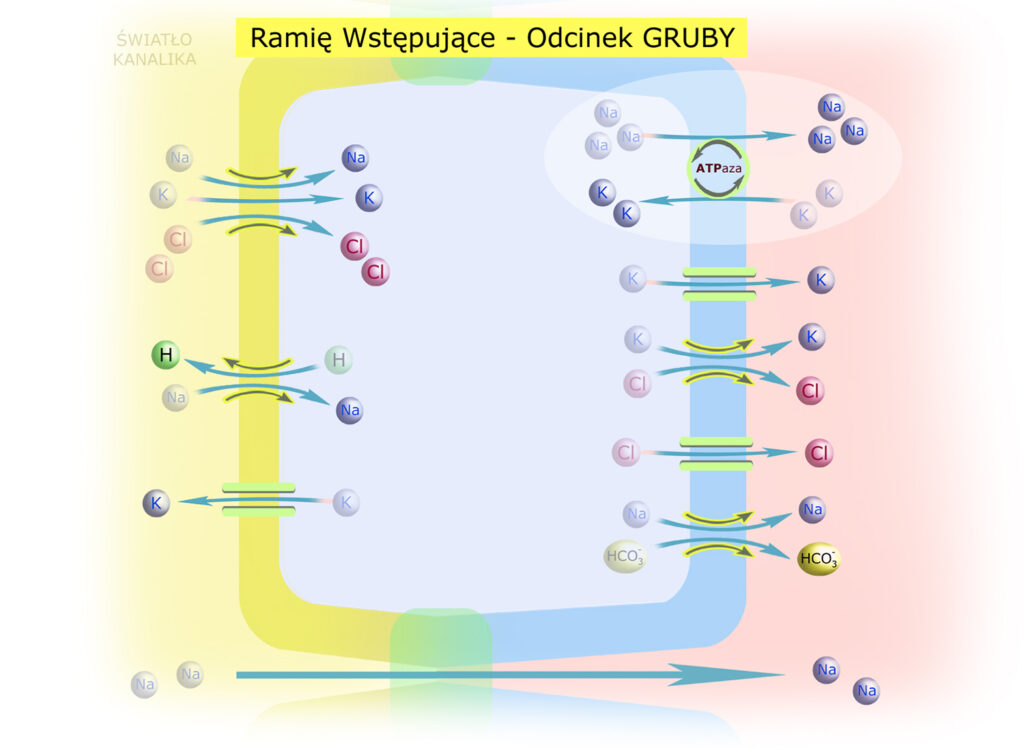
Zapewne zauważasz, że kierunek przemieszczania się jonów (np. jonów K+ na powyższym schemacie) sprawia czasem wrażenie ’awanturniczego’: z cytoplazmy do światła kanalika, z powrotem do cytoplazmy, a czasem w drugą stronę – do ppk i z powrotem…
Takie zachowanie wymuszane jest koniecznością podążania za gradientem elektrycznym – zgodnie z prawem elektroobojętności. Mówi ono, że sumy ładunków elektrycznych po obu stronach błony muszą pozostać stałe. Jeśli więc jakikolwiek kation, np. Na+, przemieszcza się na drugą stronę błony, to musi albo pociągnąć za sobą jakiś anion, np. Cl– (symport Na+/Cl–) albo wymienić się z innym kationem, np. K+ (antyport Na+/H+).
Dotyczy to obu biegunów komórki łącznie i jednocześnie: Jeśli np. Cl– lub K+ opuszcza cytoplazmę i przechodzi do ppk, to jego miejsce w cytoplazmie może zająć jon ze światła kanalika.
Podsumowując zdarzenia zachodzące w całej pętli nefronu, globalny bilans jest taki, że wchłonięciu ulega:
~10% przesączonej wody (ramię zstępujące) i
~25% przesączonego NaCl (ramię wstępujace)
Kanalik Dalszy
/dystalny/
W kanaliku dalszym woda wciąż nie jest resorbowana, więc postępuje rozcieńczenie zawartości kanalików. W końcowej części kanalika dalszego toniczność moczu kanalikowego osiąga 100 mmol/kg, jest więc 3-krotnie niższa w stosunku do toniczności przesączu kłębuszkowego (300 mmol/kg).

Podobnie jak w grubym odcinku ramienia wstępującego, w kanaliku dalszym wciąż pracuje pompa sodowo-potasowa, zmniejszając stężenie sodu w cytoplazmie. Pozwala to na wtórnie czynny transport sodu przez błonę luminalną, a także resorpcję sodu drogą paracelularną.
Zarówno w grubym odcinku ramienia wstępującego jak i w kanaliku dalszym – oprócz sodu Na+ – drogą paracelularną mogą się też wchłaniać jony potasu K+, wapnia Ca2+ i wodorowęglany HCO3–.
Kanalik Zbiorczy
Transport w kanalikach zbiorczych nie posiada prostej, jednolitej natury. Jako obszar działania mnogich mechanizmów regulacyjnych, transport przyjmuje tu różną postać, a jego charakter zależy od potrzeb organizmu. Pomijając końcowy odcinek kanalików zbiorczych (omówiony w artykule o zagęszczaniu moczu i wpływach wazopresyny), trzeba zwrócić uwagę na trzy typy komórek ścian kanalika zbiorczego. Są to komórki główne, pozostające pod wyraźnym wpływem aldosteronu, oraz komórki wstawkowe, przejawiające dwa rodzaje zachowań – zależne od tego, czy w organizmie dochodzi do niedoboru potasu, czy też nie.
Komórki Główne
Kanalika Zbiorczego
Można powiedzieć, że są to komórki wykonawcze, realizujące politykę ALDOSTERONU: resorbują sód i wydalają potas, przywracając właściwe proporcje tych kationów w przestrzeni pozakomórkowej.*
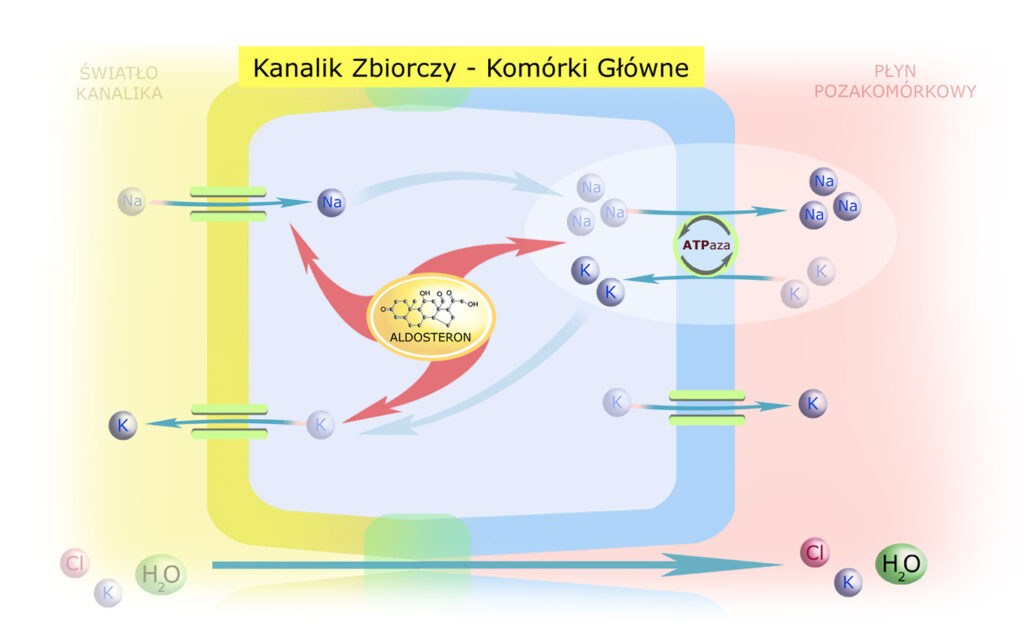
*) Aldosteron jest głównym regulatorem gospodarki sodowo-potasowej; przy niedoborze aldosteronu wydalanie sodu rośnie 6-krotnie, a w stanach hiperaldosteronizmu mocz nie zawiera sodu prawie w ogóle.
Komórki Wstawkowe
Kanalika Zbiorczego
Dla higieny rozumowania można przyjąć, że komórki wstawkowe czuwają nad transportem potasu. W warunkach prawidłowych – wydzielają potas do światła kanalika. Aktywny staje się ten podtyp komórek wstawkowych, który posiada pompę protonową w błonie antyluminalnej:
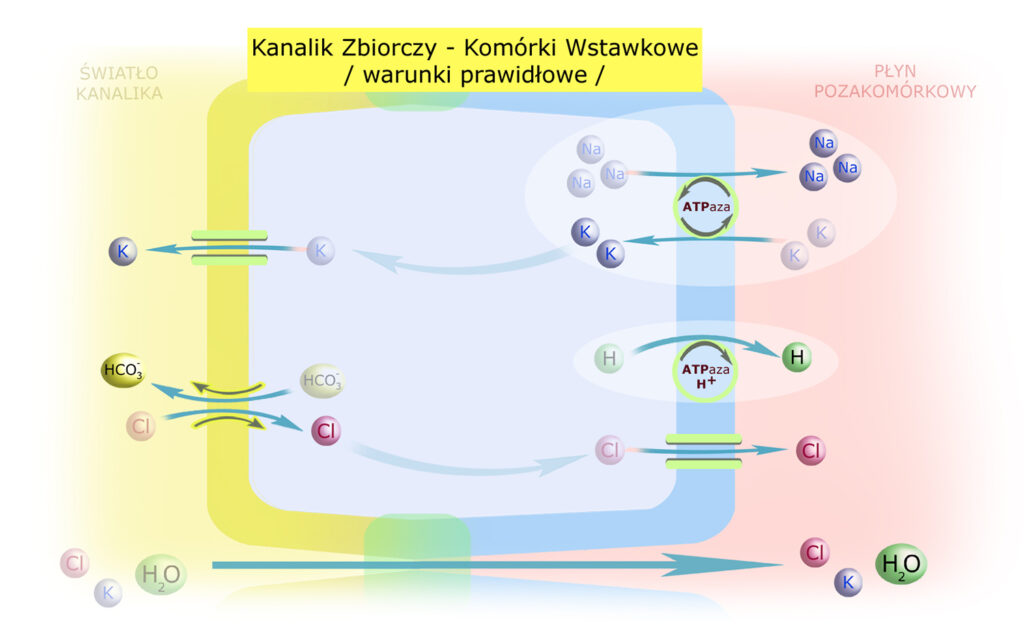
Pompa protonowa pobudza antyport Cl– / HCO3–, który wspólnie z kanałem chlorowym zapewnia resorpcję Cl–. Potas wydalany jest do światła kanalika.
W stanach niedoboru potasu aktywuje się inny podtyp komórek wstawkowych, posiadający odwrócone rozmieszczenie przenośników:
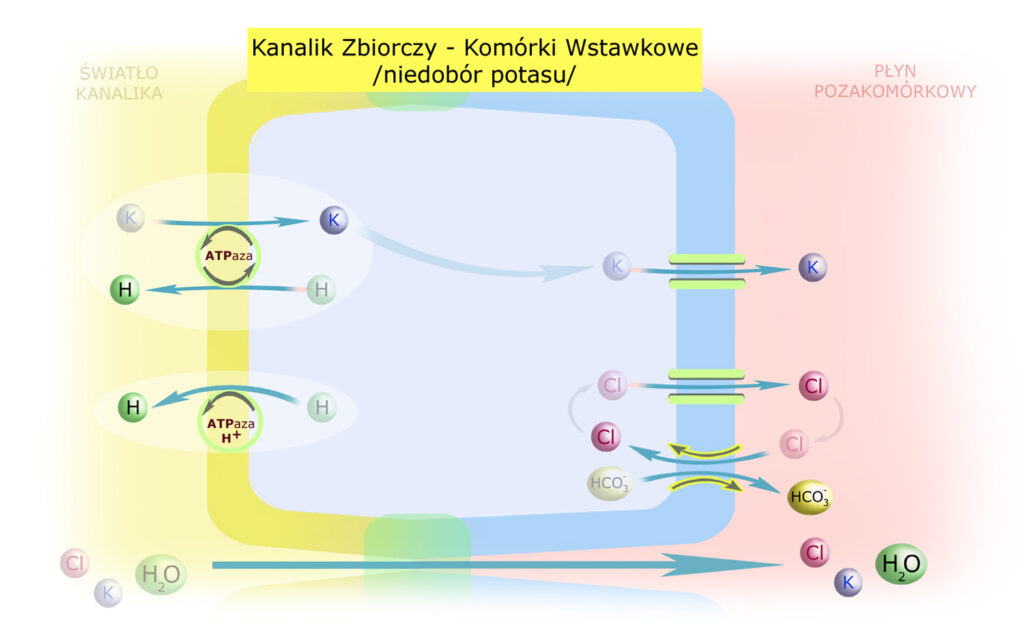
Tym razem pompa protonowa, a prócz niej też pompa protonowo-potasowa, znajdują się w błonie luminalnej, natomiast antyport Cl– / HCO3– – w antyluminalnej. Dzięki temu potas jest oszczędzany i resorbowany, a do światła kanalika wydalane są znaczne ilości jonu H+.
Transport Kanalikowy Innych Substancji
/glukoza, aminokwasy, białka, jony organiczne/
Poza utrzymywaniem stałego składu, objętości i odczynu płynów ustrojowych zadaniem nerek jest też wydalanie substancji zbędnych i oszczędzanie cennych. Rolę taką pełnią nerki np. w stosunku do glukozy.
GLUKOZA nie jest zatrzymywana przez błonę filtracyjną kłębuszków nerkowych, więc pojawia się w przesączu. W warunkach normalnych w całości jest resorbowana w początkowym odcinku kanalika bliższego (symport sodowo-glukozowy). Symport ten ma jednak swoją określoną wydajność, zwaną transportem maksymalnym glukozy, po przekroczeniu której glukoza zaczyna się pojawiać w moczu.*
*) Ten właśnie objaw stoi za wyborem nazwy dla jednej z powszechniejszych współczesnych chorób metabolicznych. W dawnych czasach całą diagnostykę laboratoryjną stanowiły zmysły lekarzy – w tym zmysł smaku. Lekarze zauważyli, że mocz niektórych pacjentów bywał słodki; ich chorobę nazwano więc cukrzycą.
Jak widzisz, wbrew powszechnym mniemaniom, nazwa tej choroby nie ma nic wspólnego z jej przyczyną, ale z objawem.
Obie nerki są w stanie zresorbować maksymalnie 375 mg glukozy w ciągu minuty – i tyle właśnie wynosi transport maksymalny glukozy: 375 mg/min (2,1 mmol/L). Stężenie glukozy w osoczu, przy którym przekraczana jest wydajność resorbcyjna kanalików – nazywamy progiem nerkowym dla glukozy. (Zwykle próg ten wynosi ~11 mmol/L = 2g/L).
AMINOKWASY również resorbowane są w kanaliku bliższym przez symport sodowy. Za symport ten odpowiada kilka przenośników, ale ich specyficzność nie jest wysoka. Np. jeden z nich transportuje aż 12 różnych aminokwasów obojętnych, inny 3 aminokwasy zasadowe + cystynę, jeszcze inny 2 aminokwasy kwaśne (kwasy asparaginowy i glutaminowy).
BIAŁKA przedostają się przez błonę filtracyjną kłębuszków w ilościach znikomych, z czego i tak 94% ulega resorpcji drogą endocytozy w kanaliku bliższym. W prawidłowym moczu wydalamy więc białko w ilości ~0,1g/24h. Proces resorpcji białka ma jednak również swoją określoną maksymalną wydajność, więc zmiany chorobowe kłębuszków mogą skutkować znacznym białkomoczem.
MOCZANY (aniony kwasu moczowego) – jako jony – filtrują się w kłębuszkach i są czynnie resorbowane w kanaliku bliższym. Gdy jednak stężenie moczanów w osoczu zwiększa się – w kanaliku bliższym dochodzi do ich czynnej sekrecji – podlegającej regulacji. Gdy regulacja ta zawodzi na którymkolwiek z etapów (filtracja/resorpcja/sekrecja) może dojść do zwiększenia stężenia moczanów w osoczu i odkładania się ich w tkankach (objawy dny moczanowej).
Do światła kanalików bliższych wydalane są też czynnie liczne kationy endogenne, takie jak hormony, autakoidy i neuroprzekaźniki (adrenalina, noradrenalina, dopamina, acetylocholina, serotonina), a także kationy egzogenne (np. niektóre leki).